ciepło
Ciepło – sposób wymiany energii wewnętrznej pomiędzy układami termodynamicznymi, zachodzący poprzez przewodzenie ciepła (przewodnictwo cieplne), konwekcję (unoszenie ciepła) i promieniowanie cieplne. Ciepło (Q) jest wielkością fizyczną określającą ilość energii wewnętrznej przekazywanej pomiędzy układami termodynamicznymi będącymi w stanie nierównowagi termicznej, co prowadzi do zmiany ich temperatury (z wyjątkiem przemian fazowych). Jednostką ciepła w układzie SI jest dżul (J).
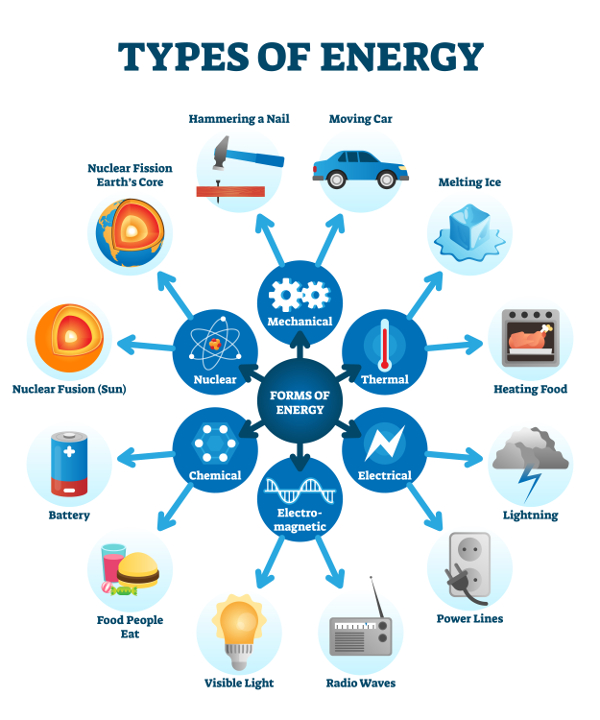
Energia wewnętrzna układu (U)
Energia wewnętrzna układu (U) definiowana jest jako całkowita energia cząstek tworzących układ termodynamiczny, składająca się z energii ruchu translacyjnego, oscylacyjnego oraz rotacyjnego cząstek układu, energii ich wzajemnych oddziaływań (międzycząsteczkowych oraz wewnątrzcząsteczkowych) oraz ich energii elektronowej i jądrowej. Energia kinetyczna ruchu układu jako całości oraz energia potencjalna w zewnętrznych polach sił przeważnie nie są uwzględniane jako części składowe energii wewnętrznej. Energia wewnętrzna układu stanowi funkcję stanu, której zmiany w danym procesie termodynamicznym zależą wyłącznie od różnicy wartości początkowej i końcowej i są niezależne od przebiegu tego procesu.
Zgodnie z zasadą zachowania energii suma energii wszystkich cząstek zamkniętego układu termodynamicznego, czyli energia wewnętrzna (U), jest stała w czasie – nie może powstać na nowo ani ulec zniszczeniu; możliwa jest tylko przemiana jednych form w inne formy energii. Zgodnie z założeniami I zasady termodynamiki zmiana energii wewnętrznej danego układu termodynamicznego jest równa sumie pracy wykonanej przez układ lub nad tym układem przez siłę zewnętrzną oraz ciepła wymienionego przez ten układ z otoczeniem:
∆ U = Q + W
gdzie:
∆ U – zmiana energii wewnętrznej układu
Q – ciepło wymienione przez układ z otoczeniem
W – praca wykonana przez układ lub nad układem przez siłę zewnętrzną
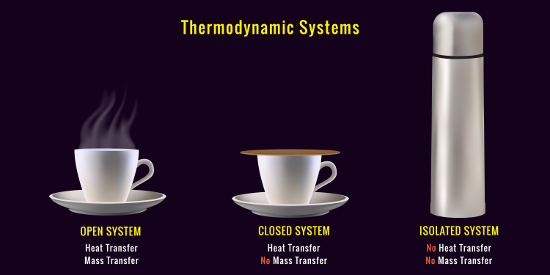
Zmiana energii wewnętrznej układu termodynamicznego nie wykonującego żadnej pracy (przemiana izochoryczna) równa jest ilości ciepła wymienionego przez układ z otoczeniem (∆ U = Q); w przypadku układu termodynamicznie izolowanego nie następuje wymiana energii z otoczeniem ani w postaci ciepła ani w postaci pracy wykonanej przez układ, w związku z czym nie następuje zmiana energii wewnętrznej tego układu (∆U = 0).
Ciepło (Q)
Ciepło jest jednym z dwóch (obok pracy) sposobów wymiany energii wewnętrznej pomiędzy układami termodynamicznymi. Proces wymiany tej energii, określany jako wymiana ciepła, polega na przekazywaniu pomiędzy układami energii nieuporządkowanych (chaotycznych) ruchów ich cząstek (przewodzenie ciepła); w przypadku pracy zmiana energii wewnętrznej danego układu odbywa się dzięki przekazaniu energii uporządkowanych ruchów cząstek. Wymiana ciepła może odbywać się również poprzez konwekcję oraz emisję promieniowania elektromagnetycznego przez wzbudzone cząstki układów. Ciepło, wraz z pracą, stanowią funkcje drogi, których wartości zależą od przebiegu procesu termodynamicznego.
Ciepło (Q) stanowi wielkość fizyczną określającą ilość energii wewnętrznej przekazywanej pomiędzy układami termodynamicznymi, znajdującymi się w stanie nierównowagi termicznej (posiadającymi różne temperatury), co prowadzi do zmiany ich temperatury (ogrzania bądź ochłodzenia) oraz ustalenia się równowagi termicznej pomiędzy tymi układami. Wyjątek stanowią przemiany (przejścia) fazowe przebiegające w warunkach stałej temperatury, prowadzące np. do zmiany stanu skupienia cząstek układu (np. topnienie lodu, krzepnięcie wody).
Ciepło dostarczone do zamkniętego układu termodynamicznego, zgodnie z treścią I zasady termodynamiki, powoduje zmianę energii wewnętrznej tego układu oraz wykorzystywane jest do wykonania przez ten układ pracy przeciwko siłom zewnętrznym:
∆ Q = ∆ U + W
gdzie:
∆ Q – ciepło dostarczone do układu
∆ U – zmiana energii wewnętrznej układu
W – praca wykonana przez układ przeciwko siłom zewnętrznym
Jednostką ciepła w układzie SI jest dżul (J); często używanymi jednostkami spoza układu SI są kalorie (cal) (1 cal = 4,1868 J, zatem: 1 J = 0,238846 cal) oraz brytyjska jednostka ciepła (BTU) (1 BTU = 1055,05585262 J).
Wymiana ciepła
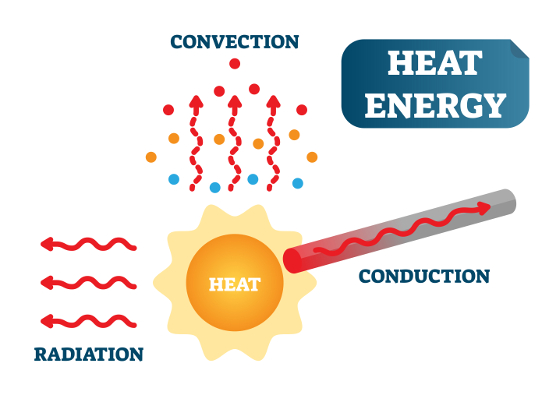
Wymiana ciepła, określana również mianem transportu ciepła bądź cieplnego przepływu energii, odbywa się pomiędzy układami termodynamicznymi będącymi w nierównowadze termicznej poprzez przewodzenie ciepła (układy znajdujące się w bezpośrednim kontakcie) bądź konwekcję (unoszenie ciepła) lub promieniowanie cieplne (pozostałe układy termodynamiczne).
Przewodzenie ciepła (przewodnictwo cieplne) jest procesem wymiany ciepła pomiędzy układami termodynamicznymi o różnej temperaturze, polegającym na przekazywaniu energii kinetycznej nieuporządkowanego (chaotycznego) ruchu cząsteczek tych układów w wyniku ich bezpośrednich oddziaływań (zderzeń) z układu termodynamicznego o wyższej temperaturze do układu termodynamicznego o temperaturze niższej.
Konwekcja (unoszenie ciepła) polega na przenoszeniu energii cieplnej pomiędzy układami termodynamicznymi dzięki ruchowi makroskopowych ilości płynów (cieczy lub gazów), które zachodzą pod wpływem oddziaływania czynników zewnętrznych (konwekcja wymuszona, konwekcja sztuczna) lub wskutek różnicy gęstości pomiędzy tymi układami wynikającej z różnicy ich temperatur (konwekcja swobodna, konwekcja naturalna).
Wymiana ciepła między układami termodynamicznymi poprzez promieniowanie cieplne (promieniowanie termiczne) polega na emisji promieniowania elektromagnetycznego przez wzbudzone atomów lub cząsteczek tych układów, w wyniku zachodzących ruchów cieplnych (termicznych) tych cząstek.